Online first
Bieżący numer
Archiwum
O czasopiśmie
Polityka etyki publikacyjnej
System antyplagiatowy
Instrukcje dla Autorów
Instrukcje dla Recenzentów
Rada Redakcyjna
Komitet Redakcyjny
Recenzenci
Wszyscy recenzenci
2025
2024
2023
2022
2021
2020
2019
2018
2017
2016
Kontakt
Bazy indeksacyjne
Klauzula przetwarzania danych osobowych (RODO)
PRACA ORYGINALNA
Ocena wpływu terapii liraglutydem na masę ciała i insulinooporność.
1
National Medical Institute of the Ministry of the Interior and Administration, Warsaw, Poland
Autor do korespondencji
Waldemar Wierzba
National Medical Institute of the Ministry of the Interior and Administration, Warsaw, Poland
National Medical Institute of the Ministry of the Interior and Administration, Warsaw, Poland
Med Og Nauk Zdr. 2023;29(4):290-292
SŁOWA KLUCZOWE
DZIEDZINY
STRESZCZENIE
Wprowadzenie i cel:
Insulinooporność to stan zmniejszonej wrażliwości tkanek na działanie insuliny pomimo prawidłowego lub podwyższonego poziomu tego hormonu w surowicy. Liraglutyd (agonista receptora GLP-1) stymuluje wydzielanie insuliny z trzustki, jednocześnie zmniejszając nadmierne uwalnianie glukagonu. Analogi GLP-1 mają wyjątkowo korzystny wpływ na odchudzanie poprzez stymulację wydzielania insuliny bez nadmiernego wzrostu poziomu cukru we krwi. Zbadaliśmy wpływ liraglutydu na wskaźnik masy ciała i insulinooporność u osób z nadwagą i otyłością, którenie chorują na cukrzycę.
Materiał i metody:
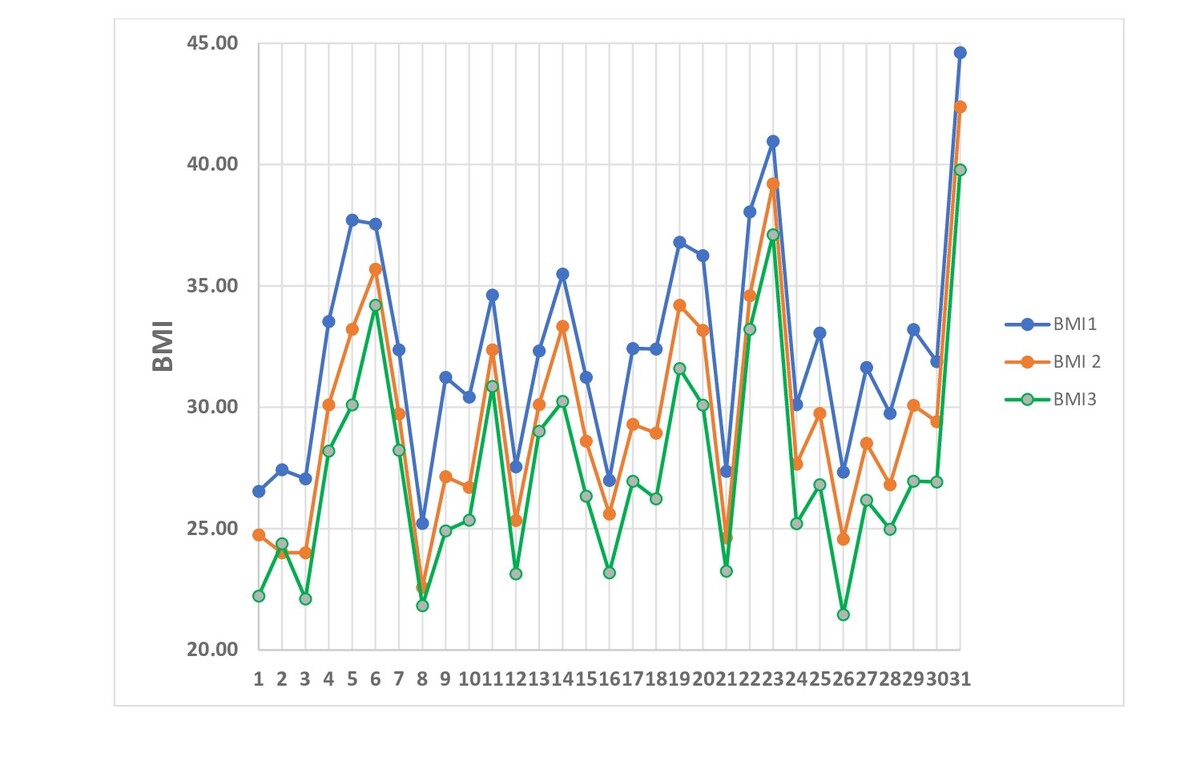
W badaniu wzięło udział 31 kobiet z nadwagą i otyłością (BMI ≥ 25), które były leczone liraglutydem w latach 2021–2022. Liraglutyd w dawce 3,0 mg stosowano jako dodatek do terapii behawioralnej, która obejmowała dietę niskokaloryczną i program ćwiczeń. W badaniu wykorzystano następujące informacje o uczestniczkach: wartość BMI, poziomy glukozy i insuliny oraz wskaźnik HOMA przed i podczas leczenia liraglutydem. Masę ciała określono i badania krwi przeprowadzono na początku leczenia (BMI1, HOMA1), a także po 3 (BMI2, HOMA2) i 6 miesiącach (BMI3, HOMA3) leczenia w celu zaobserwowania zmian.
Wyniki:
Średni wiek uczestniczek badania wynosił 38,32 ± 7,41 lat. Zmiany BMI od wartości wyjściowej (32,36 ± 4,56) do niższej (27,46 ± 4,45), co nastąpiło w okresie 6 miesięcy, wiązały się ze znaczną redukcją masy ciała (p < 0,001). Zmiany wskaźnika HOMA od wartości wyjściowej (4,73 ± 1,48) do tej uzyskanej w ciągu 3 (3,59 ± 1,26) i 6 miesięcy (2,47 ± 0,91) były istotne statystycznie (p < 0,03; p < 0,001).
Wnioski:
Liraglutyd stanowi obiecującą redukcję masy ciała i otyłości u pacjentów bez cukrzycy jako uzupełnienie terapii behawioralnej. Agonisty receptora GLP-1, reprezentujący nową klasę leków przeciwcukrzycowych, niewątpliwie oferują wyjątkowe korzyści pacjentom z nadwagą lub otyłością. Stosowanie liraglutydu w dawce 3,0 mg wiązało się ze znaczną redukcją masy ciała i obniżeniem insulinooporności.
Insulinooporność to stan zmniejszonej wrażliwości tkanek na działanie insuliny pomimo prawidłowego lub podwyższonego poziomu tego hormonu w surowicy. Liraglutyd (agonista receptora GLP-1) stymuluje wydzielanie insuliny z trzustki, jednocześnie zmniejszając nadmierne uwalnianie glukagonu. Analogi GLP-1 mają wyjątkowo korzystny wpływ na odchudzanie poprzez stymulację wydzielania insuliny bez nadmiernego wzrostu poziomu cukru we krwi. Zbadaliśmy wpływ liraglutydu na wskaźnik masy ciała i insulinooporność u osób z nadwagą i otyłością, którenie chorują na cukrzycę.
Materiał i metody:
W badaniu wzięło udział 31 kobiet z nadwagą i otyłością (BMI ≥ 25), które były leczone liraglutydem w latach 2021–2022. Liraglutyd w dawce 3,0 mg stosowano jako dodatek do terapii behawioralnej, która obejmowała dietę niskokaloryczną i program ćwiczeń. W badaniu wykorzystano następujące informacje o uczestniczkach: wartość BMI, poziomy glukozy i insuliny oraz wskaźnik HOMA przed i podczas leczenia liraglutydem. Masę ciała określono i badania krwi przeprowadzono na początku leczenia (BMI1, HOMA1), a także po 3 (BMI2, HOMA2) i 6 miesiącach (BMI3, HOMA3) leczenia w celu zaobserwowania zmian.
Wyniki:
Średni wiek uczestniczek badania wynosił 38,32 ± 7,41 lat. Zmiany BMI od wartości wyjściowej (32,36 ± 4,56) do niższej (27,46 ± 4,45), co nastąpiło w okresie 6 miesięcy, wiązały się ze znaczną redukcją masy ciała (p < 0,001). Zmiany wskaźnika HOMA od wartości wyjściowej (4,73 ± 1,48) do tej uzyskanej w ciągu 3 (3,59 ± 1,26) i 6 miesięcy (2,47 ± 0,91) były istotne statystycznie (p < 0,03; p < 0,001).
Wnioski:
Liraglutyd stanowi obiecującą redukcję masy ciała i otyłości u pacjentów bez cukrzycy jako uzupełnienie terapii behawioralnej. Agonisty receptora GLP-1, reprezentujący nową klasę leków przeciwcukrzycowych, niewątpliwie oferują wyjątkowe korzyści pacjentom z nadwagą lub otyłością. Stosowanie liraglutydu w dawce 3,0 mg wiązało się ze znaczną redukcją masy ciała i obniżeniem insulinooporności.
Introduction and objective:
Insulin resistance is a state of reduced tissue sensitivity to insulin action despite normal or elevated serum insulin levels. Liraglutide (a GLP-1 receptor agonist) stimulates insulin secretion from the pancreas while decreasing excessive glucagon release. GLP-1 analogues have a unique beneficial effect on weight loss by stimulating insulin secretion without increasing blood sugar levels excessively. The aim of the study was to investigate the effects of liraglutide on body mass index and insulin resistance in overweight and obese non-diabetic individuals.
Material and methods:
The study involved 31 overweight and obese women (BMI of ≥25 kg/m2) who received liraglutide treatment between 2021–2022. Liraglutide 3.0 mg was used as an adjunct to behavioural therapy, which included a lowcalorie diet and exercise programme. The study collected BMI, glucose and insulin levels, and HOMA index before and during liraglutide treatment. Body weight and blood tests were examined at baseline (BMI1, HOMA1), as well as at 3 (BMI2, HOMA2), and 6 months (BMI3, HOMA3) of treatment to observe any changes.
Results:
Average age of participants – 38.32±7.41 years. Changes in BMI from baseline (32.36±4.56 kg/m²) to 6 months (27.46±4.45kg/m²) were associated with a significant reduction in weight (p <0.001). Changes in HOMA index from baseline (4.73±1.48) to 3 (3.59±1.26) and 6 months (2.47±0.91) were statistically significant (p <0.03, p < 0.001).
Conclusions:
Liraglutide represents a promising option for reducing body weight and obesity in non-diabetic patients as an adjunct to behavioural therapy. Agonists GLP-1 receptor, representing a new class of antidiabetic drug, undoubtedly offer unique benefits for overweight or obesity patients. Liraglutide in 3.0 mg use was associated with a significant weight reduction and lowering of insulin resistance.
Insulin resistance is a state of reduced tissue sensitivity to insulin action despite normal or elevated serum insulin levels. Liraglutide (a GLP-1 receptor agonist) stimulates insulin secretion from the pancreas while decreasing excessive glucagon release. GLP-1 analogues have a unique beneficial effect on weight loss by stimulating insulin secretion without increasing blood sugar levels excessively. The aim of the study was to investigate the effects of liraglutide on body mass index and insulin resistance in overweight and obese non-diabetic individuals.
Material and methods:
The study involved 31 overweight and obese women (BMI of ≥25 kg/m2) who received liraglutide treatment between 2021–2022. Liraglutide 3.0 mg was used as an adjunct to behavioural therapy, which included a lowcalorie diet and exercise programme. The study collected BMI, glucose and insulin levels, and HOMA index before and during liraglutide treatment. Body weight and blood tests were examined at baseline (BMI1, HOMA1), as well as at 3 (BMI2, HOMA2), and 6 months (BMI3, HOMA3) of treatment to observe any changes.
Results:
Average age of participants – 38.32±7.41 years. Changes in BMI from baseline (32.36±4.56 kg/m²) to 6 months (27.46±4.45kg/m²) were associated with a significant reduction in weight (p <0.001). Changes in HOMA index from baseline (4.73±1.48) to 3 (3.59±1.26) and 6 months (2.47±0.91) were statistically significant (p <0.03, p < 0.001).
Conclusions:
Liraglutide represents a promising option for reducing body weight and obesity in non-diabetic patients as an adjunct to behavioural therapy. Agonists GLP-1 receptor, representing a new class of antidiabetic drug, undoubtedly offer unique benefits for overweight or obesity patients. Liraglutide in 3.0 mg use was associated with a significant weight reduction and lowering of insulin resistance.
Szydlarska D, Jakubowska A, Owoc J, Wierzba W. Evaluation of the effect of liraglutide therapy on body weight and insulin resistance. Med
Og Nauk Zdr. 2023; 290–292. doi: 10.26444/monz/176898
REFERENCJE (12)
1.
Szydlarska D, Machaj M, Jakimiuk A. History of discovery of polycystic ovary syndrome. AdvClinExp Med. 2017 May Jun;26(3):555–558.
2.
Shin-Hae L, Shi-Young P, Cheol SC. Insulin Resistance: From Mechanism to Therapeutic Strategies. DiabetesMetab J. 2022 Jan;46(1):15–37.
3.
Donna H, Ryan S, Ryan Y. Weight Loss and Improvement in Comorbidity: Differences at 5%, 10%, 15%, and Over. CurrObes Rep. 2017 Jun;6(2):187–194.
4.
Bray GA, Heisel WE, Afshin A, et al. The Science of Obesity Management: An Endocrine Society Scientific Statement. Endocr Rev. 2018 Apr;39(2):79–132.
5.
Overgaard RV, Petri KC, Lisbeth V, et al. Liraglutide 3.0 mg for Weight Management: A Population Pharmacokinetic Analysis. Clin Pharmacokinet. 2016;55(11):1413–1422.
6.
Pei Zhang, Yu Liu, Yuan Ren, Jie Bai, et al. The efficacy and safety of liraglutide in the obese, non-diabetic individuals: a systemic review and meta-analysis. Afr Health Sci. 2019 Sep;19(3):2591–2599.
7.
Garber AJ, Henry R, Ratner R, et al. Liraglutide versus glimepiride monotherapy for type 2 diabetes (lead-3 mono): a randomised, 52-week, phase iii, double-blind, parallel-treatment trial. Lancet, 2009;373:473–481.
8.
Astrup A, Rossner S, Van Gaal L, et al. Effects of Liraglutide in the treatment of obesity: a randomised, double-blind, placebo-controlled study. Lancet. 2009;374:1606–1616.
9.
Sharma A, Ambrosy AP, DeVore AD, et al. Liraglutide and weight loss among patients with advanced heart failure and a reducedejection fraction: insights from the FIGHT trial. ESC Heart Fail. 2018 Dec;5(6):1035–1043.
10.
Garvey WT, Birkenfeld AL, Dicker D, Mingrone G, et al. Efficacy and Safety of Liraglutide 3.0 mg in Individuals With Overweight or Obesity and Type 2 Diabetes Treated With Basal Insulin: The SCALE Insulin Randomized Controlled Trial. Diabetes Care. 2020 May;43(5):1085–1093.
11.
Kadouh H, Chedid V, Halawi H, et al. GLP-1 Analog Modulates Appetite, Taste Preference, Gut Hormones, and Regional Body Fat Stores in Adults with Obesity. J Clin Endocrinol Metab. 2020; 105(5): 1552–1563.
12.
Cosentino F, Ceriello A, Baeres FMM, et al. Addressing cardiovascular risk in type 2 diabetes mellitus: a report from the European Society of Cardiology Cardiovascular Roundtable. Eur Heart J. 2019 Sep 7;40(34):2907–2919.
Udostępnij
ARTYKUŁ POWIĄZANY
Przetwarzamy dane osobowe zbierane podczas odwiedzania serwisu. Realizacja funkcji pozyskiwania informacji o użytkownikach i ich zachowaniu odbywa się poprzez dobrowolnie wprowadzone w formularzach informacje oraz zapisywanie w urządzeniach końcowych plików cookies (tzw. ciasteczka). Dane, w tym pliki cookies, wykorzystywane są w celu realizacji usług, zapewnienia wygodnego korzystania ze strony oraz w celu monitorowania ruchu zgodnie z Polityką prywatności. Dane są także zbierane i przetwarzane przez narzędzie Google Analytics (więcej).
Możesz zmienić ustawienia cookies w swojej przeglądarce. Ograniczenie stosowania plików cookies w konfiguracji przeglądarki może wpłynąć na niektóre funkcjonalności dostępne na stronie.
Możesz zmienić ustawienia cookies w swojej przeglądarce. Ograniczenie stosowania plików cookies w konfiguracji przeglądarki może wpłynąć na niektóre funkcjonalności dostępne na stronie.